2024年5月1日,由中國醫藥質量管理協會發布的《研究者發起的抗腫瘤體細胞臨床研究細胞制劑制備和質量控制規范》(T/CQAP 3014—2024)標準(以下簡稱“標準”)將正式實施。

該標準旨在制定適應中國國情、符合企業實際、標準統一規范的抗腫瘤體細胞臨床研究質量控制體系。
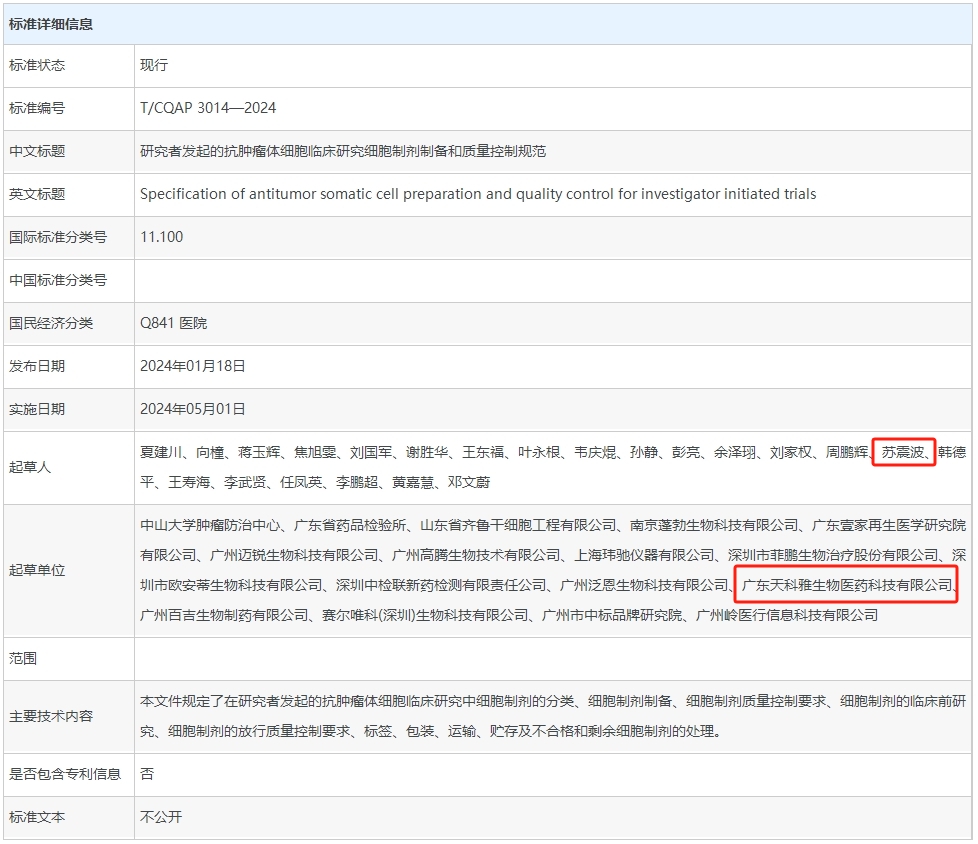
該標準由22位行業專家共同起草,共涉及17家單位。
中山大學腫瘤防治中心主任導師兼中國醫藥質量管理協會細胞治療質量控制與研究專業委員會主任委員夏建川、實驗研究部副研究員向橦、廣東省藥品檢驗所一級主任科員蔣玉輝、廣東天科雅生物醫藥科技有限公司等參與起草,助力推動中國抗腫瘤體細胞臨床研究。
標準的主要技術內容規定了在研究者發起的抗腫瘤體細胞臨床研究中細胞制劑的分類,細胞制劑制備,細胞制劑質量控制要求,細胞制劑的臨床前研究,細胞制劑的放行質量控制要求、標簽、包裝、運輸、貯存及不合格和剩余細胞制劑的處理。
2023年10月27日,天科雅生物參與了由中國醫藥質量管理協會組織、中山大學腫瘤防治中心牽頭發起的《研究者發起的抗腫瘤體細胞臨床研究細胞制劑制備和質量控制規范》團體標準審查會暨“中國醫藥質量管理協會抗腫瘤藥物與細胞藥物臨床研究”調研會,并就本行業未來發展提出意見和建議,推動體細胞質量控制規范和標準建立。
作為國內細胞行業的重要推動者,天科雅生物專注于腫瘤免疫細胞治療技術的創新性研發和產業化,未來也將會進一步助推中國細胞治療臨床研究相關工作的規范化、標準化、科學化及中國細胞治療相關技術高質量發展。


 中文
中文
 中文
中文








 0
0





